马志明
慢性肺曲霉病的定义
资源受限环境下CPA的诊断标准(Case Definition of Chronic Pulmonary Aspergillosis in Resource-Constrained Settings)
CPA分类
不同CPA分型的诊断标准
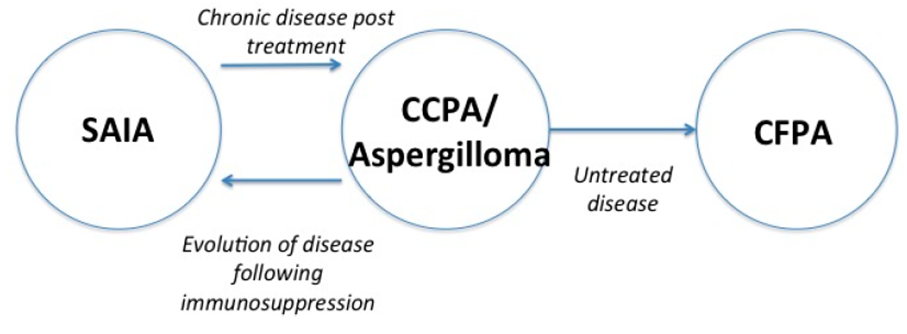
不同CPA类型之间的演变
CPA与非结核分枝杆菌肺病(NTMPD)
NTMPD后CPA流行病学
NTMPD后CPA发病机制
NTMPD后CPA风险因素
NTM菌种与CPA风险
NTMPD后CPA临床表现
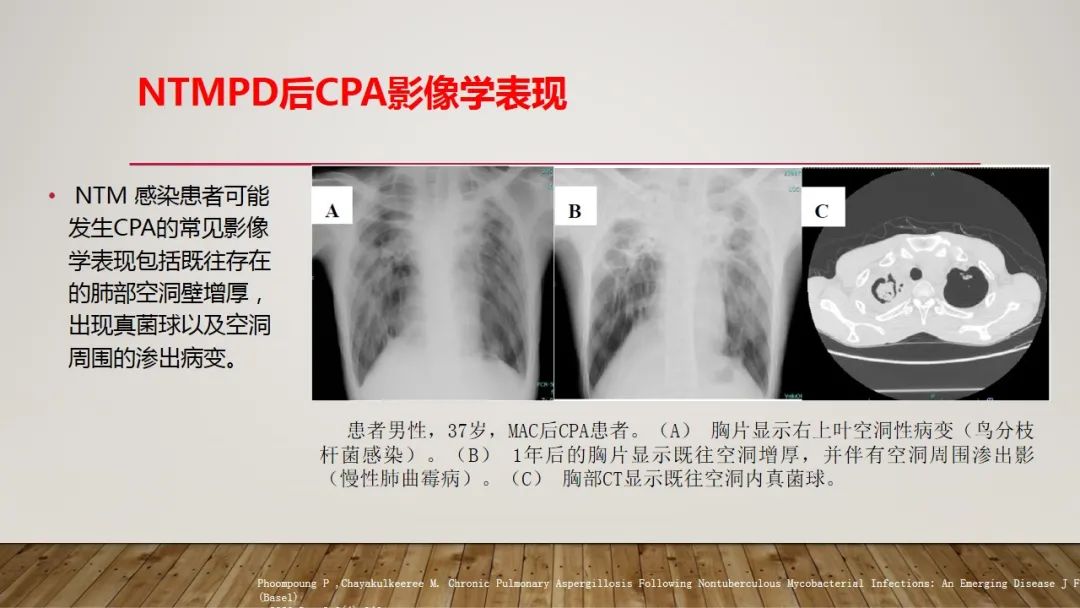
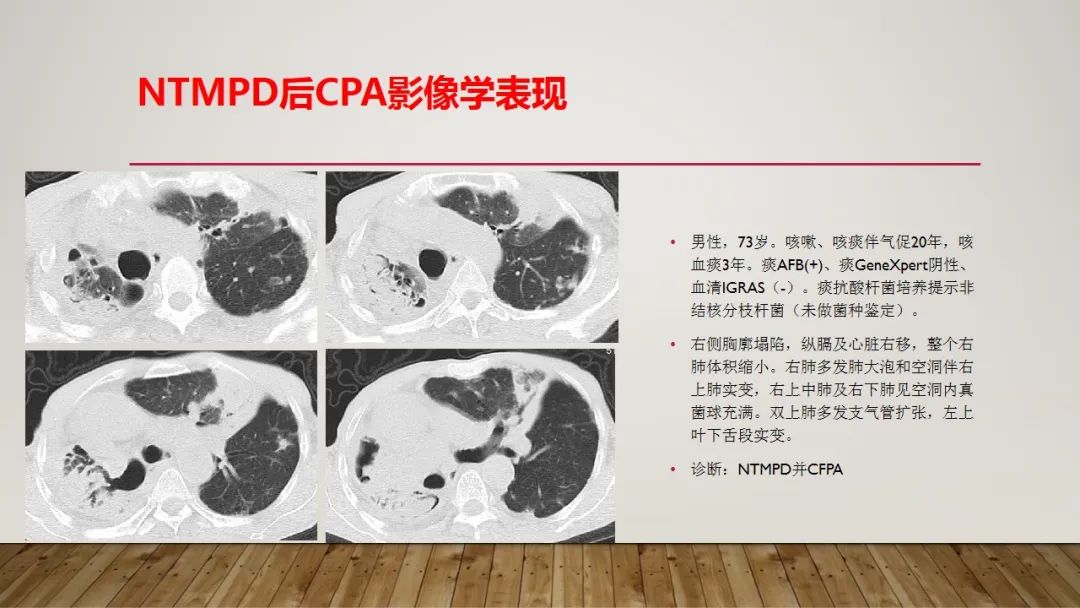
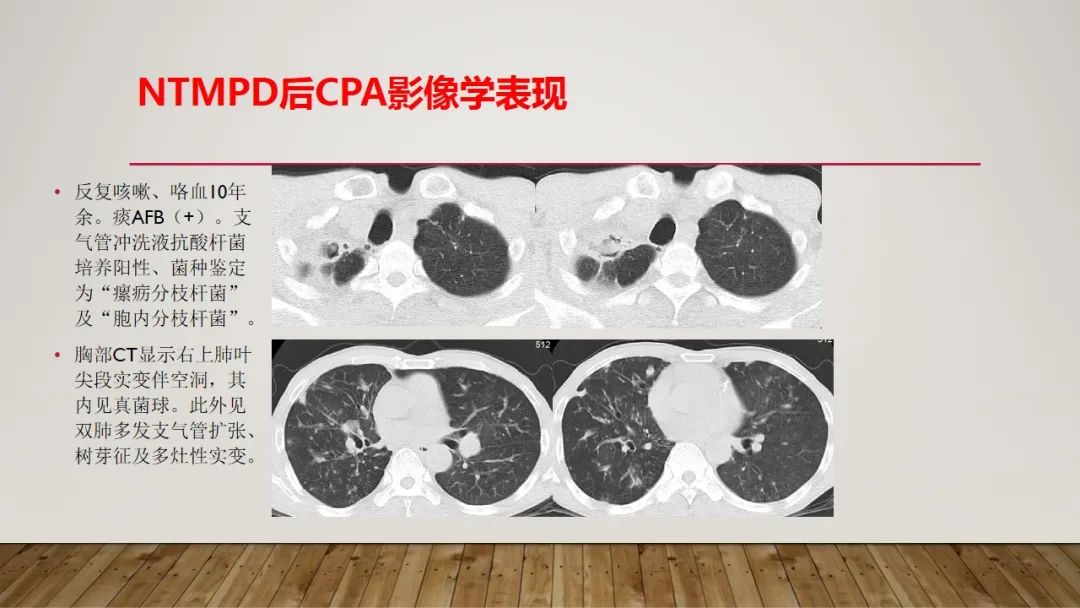
NTMPD后CPA影像学表现

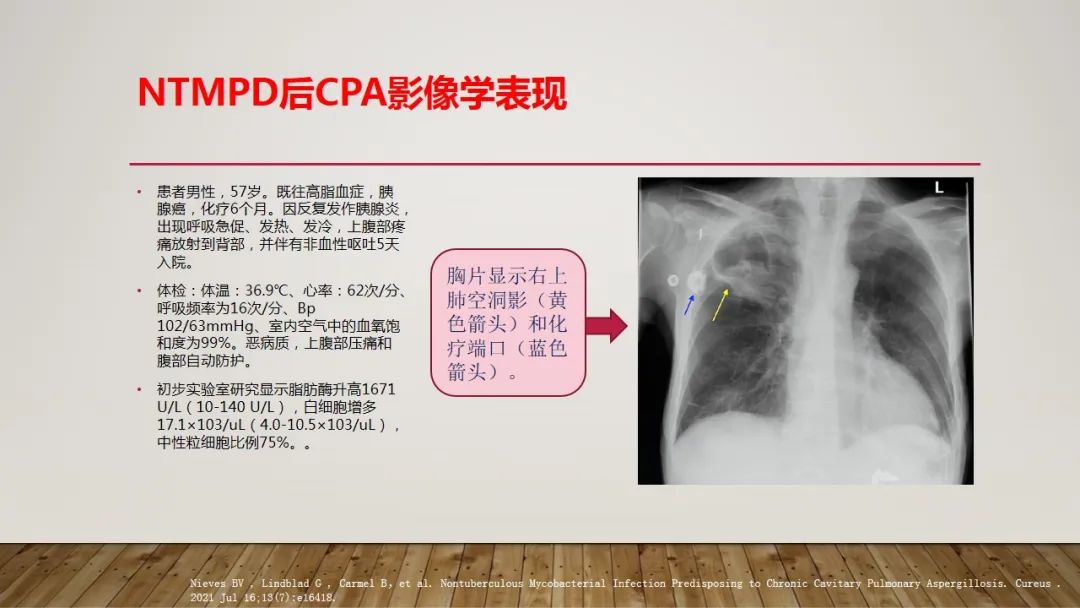
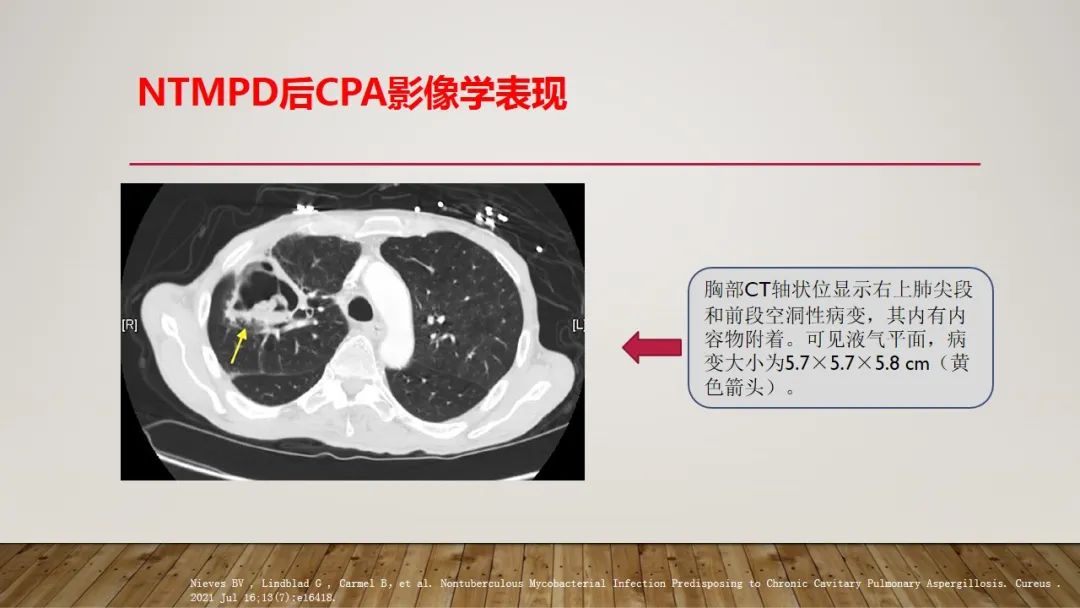
NTMPD后CPA诊断
NTMPD后CPA治疗
2015 ESCMID/ERS临床指南推荐
CPA口服三唑类药物治疗

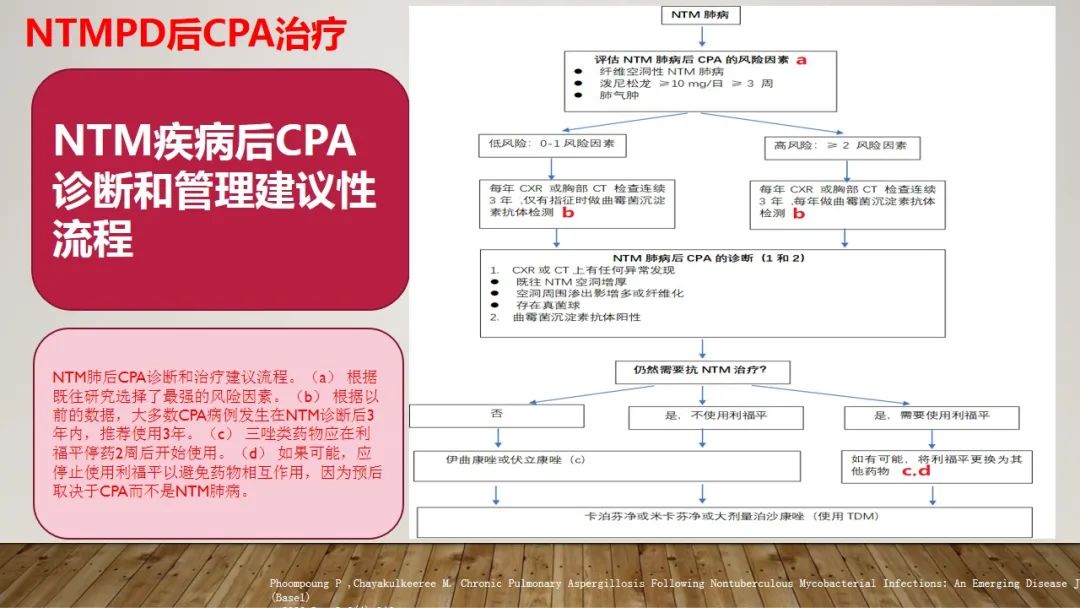
NTMPD后CPA预后
肺结核后CPA与NTM肺病后CPA的比较
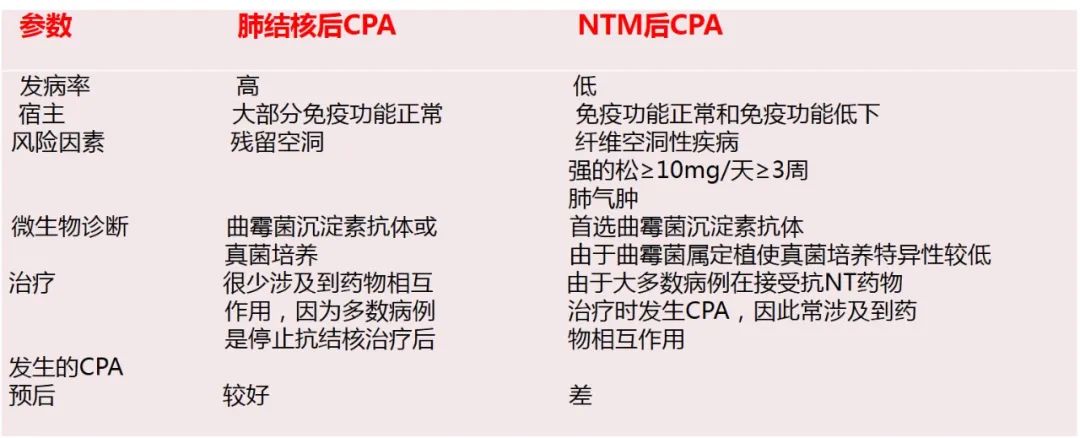
结论
目前研究的局限性及未来研究
参考文献:略