
Elizabeth Alexander, MD, MSc; Lisa Goldberg, MS; Anita F. Das, PhD; Gregory J. Moran, MD; Christian Sandrock, MD; Leanne B. Gasink, MD; Patricia Spera, PhD; Carolyn Sweeney, BS; Susanne Paukner, PhD; Wolfgang W. Wicha, MSc; Steven P. Gelone, PharmD; Jennifer Schranz, MD
科学问题:
肺炎是导致住院的最常见原因,也是感染性疾病中的主要死亡原因。社区获得性细菌性肺炎(CABP)的常见病原体包括肺炎链球菌、金黄色葡萄球菌、流感嗜血杆菌、卡他莫拉菌,以及非典型病原体、肺炎支原体、肺炎衣原体和嗜肺军团菌。目前的一线 CABP 治疗包括大环内酯类、β-内酰胺类或氟喹诺酮类。
研究监测发现肺炎链球菌和金黄色葡萄球菌分离株对治疗 CABP 抗菌药的敏感性有普遍降低的趋势,包括抗肺炎链球菌的口服青霉素、大环内酯类和叶酸通路抑制剂,以及抗金黄色葡萄球菌(尤其是耐甲氧西林的金黄色葡萄球菌)的大环内酯类和氟喹诺酮类。由于细菌耐药率较高,加上氟喹诺酮类相关安全性问题不断增加,需要新的治疗选择(临床问题)。
Lefamulin 是首款获批用于人体静脉和口服给药的截短侧耳素抗菌药。Lefamulin 对最常见的 CABP 病原体有抗菌活性,包括一些对其他抗菌药耐药的菌株。
鉴于前期有效的结果,为进一步验证 Lefamulin(新型抗菌药物)与莫西沙星(选作标准治疗)相比的疗效和安全性(科学问题),开展本次试验,以比较每日两次口服 Lefamulin 治疗 5 天与每日一次口服莫西沙星治疗 7 天的疗效和安全性(研究目的)。
摘要:
重要性:由于标准抗菌药治疗的耐药性和安全性问题不断增加,因此需要新的抗菌药来治疗社区获得性细菌性肺炎(CABP)。
目的:评价 Lefamulin 口服 5 天方案治疗 CABP 患者的疗效和不良事件。
设计、背景和受试者:在 19 个国家 99 家研究中心进行的一项 III 期、随机、非劣效临床试验,入组符合以下标准的受试者: PORT 风险级别为 II、III 或 IV 级的 ≥ 18 岁的成人;经影像学证实肺炎;急性疾病;≥ 3 种 CABP 症状;≥ 2 个生命体征异常。首例患者访视日期为 2016 年 8 月 30 日,随访持续 30 天,末次随访访视日期为 2018 年 1 月 2 日。
治疗:患者以 1:1 的比例随机接受口服 Lefamulin(600 mg 每 12 小时一次,持续 5 天;n = 370)或莫西沙星(400 mg 每 24 小时一次,持续 7 天;n = 368)。
主要评估结果 美国食品药品管理局(FDA)规定的主要终点为意向治疗(ITT)人群(所有随机分组患者)中任一研究药物首次给药后 96 小时的早期临床有效率。有效患者定义符合以下标准:存活,≥ 2/4 种 CABP 症状出现改善,任何 CABP 症状未恶化,针对当前 CABP 发作,未接受任何非研究抗菌药物。欧洲药品管理局规定的共同主要终点(FDA 规定的次要终点)是在治愈评估时(末次给药后 5-10 天)基于改良 ITT 人群(译者注:)和疗效明确的人群(译者注:)的临床疗效。早期临床有效和研究者评估的临床疗效的非劣效性界值为 10%。
结果:在 738 名进行随机分组的患者中,(平均年龄,57.5 岁;351 例女性 [47.6%];360 例 PORT 风险级别为 III 或 IV 级 [48.8%]),707 例(95.8%)完成了试验。
表 1. 意向治疗人群的人口统计学和基线特征

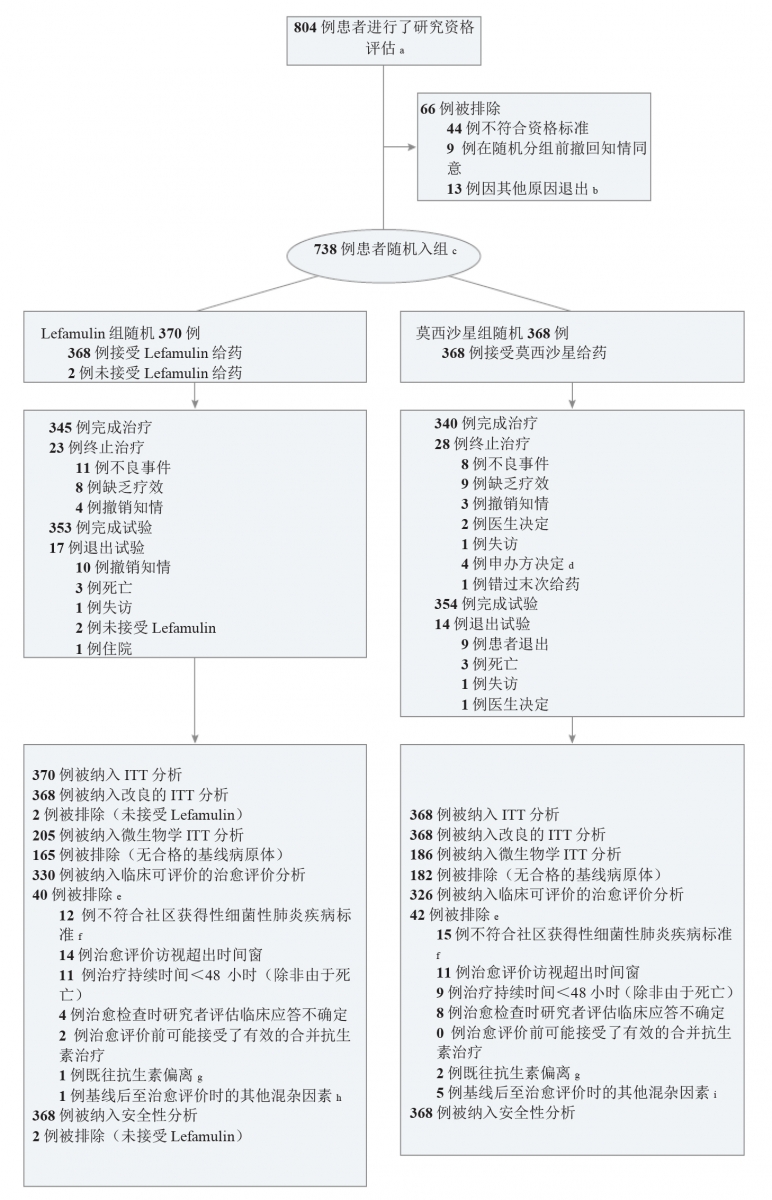
图.LEAP 2 试验中的患者招募、随机分组和随访
ITT 分析集中,Lefamulin 组的早期临床有效率为 90.8%,莫西沙星组为 90.8%(差异为 0.1%[单侧 97.5% CI,–4.4% 至∞])。在改良的 ITT 人群中, Lefamulin 组研究者评估的临床有效率为 87.5%,莫西沙星组为 89.1%(差异为–1.6%[单侧 97.5% CI,–6.3% 至∞]),在临床可评价人群中,在治愈评估时(末次给药后 5-10 天)Lefamulin 组和莫西沙星组临床有效率分别为 89.7% 和 93.6%(差异为–3.9%[单侧 97.5% CI,–8.2% 至∞])。
表 2. 意向治疗(ITT)人群的早期临床有效,在改良 ITT 人群和临床疗效明确人群中治愈评估时的临床有效

最常报告的治疗后出现的不良事件为胃肠系统事件(腹泻:Lefamulin 组 45/368[12.2%];莫西沙星组 4/368[1.1%];恶心:Lefamulin 组 19/368[5.2%];莫西沙星组 7/368[1.9%])。治疗期间报告的大多数不良事件的严重程度为轻度或中度(表 4),无腹泻病例导致研究药物停药。
表 4. 在评估安全性的人群中治疗期间出现的不良事件分布(TEAE)

试验注册 ClinicalTrials.gov 标识符:NCT02813694;欧洲临床试验标识符:2015-004782-92
结论和意义 在 CABP 患者中,在首次给药后 96 小时的早期有效率方面,5 天口服 Lefamulin 非劣效于 7 天口服莫西沙星。
安全性
口服 Lefamulin 通常耐受良好;尽管 Lefamulin 治疗组报告胃肠系统相关治疗中出现的不良事件的患者百分比高于莫西沙星组,但 Lefamulin 组中所有胃肠系统相关治疗中出现的不良事件严重程度均为轻度至中度,很少导致研究药物停药。Lefamulin 组 12.2% 的患者和莫西沙星组 1.1% 的患者报告了轻度或中度腹泻。Lefamulin 组最常见不良事件是胃肠系统不良事件,主要集中在开始口服治疗时。
要点
问题:在社区获得性细菌性肺炎的管理中,5 天口服 Lefamulin 是否非劣于 7 天口服莫西沙星?
结果:在本项纳入 738 例患者的随机临床试验中,Lefamulin 组研究药物首次给药后 96 小时(24 小时窗口期内)的早期有效率为 90.8%,莫西沙星组为 90.8%,该差异满足非劣效性界值 10%。
意义:此项研究证实了口服 Lefamulin 治疗社区获得性细菌性肺炎非劣于口服莫西沙星。
读后感:
作为今年治疗社区获得细菌性肺炎新药的重磅研究之一(另一项为 Omadacycline, N Engl J Med 2019;380:517-27),我们可以发现其有如下几个共同特点:适应症为治疗 CABP,研究设计为非劣效的 RCT,对照组为莫西沙星,结果证实疗效不差于莫西沙星,安全性与对照组相当,研究终点设计为早期临床起效。
此处特别想要指出的是治疗 CABP 的 RCT 研究为何设计为非劣效设计。目前门诊和住院社区获得性肺炎一旦诊断明确,不同抗菌药物治疗策略上的获益相差并不明显,因此针对社区获得性肺炎的研究目前大多设计为非劣效或等效。部分研究者提到 RCT 往往首先预想的结果就是干预组优于对照组,而不曾细问本研究所要评价的干预措施与目前标准治疗相比,是否真的有明显获益。
该研究设计和其他方面考量体现了目前的最高水平,若有涉及社区获得细菌性肺炎的研究者,在设计肺炎相关研究时,可以参考相关的设计思路。
最后,目前临床使用莫西沙星治疗下呼吸道感染非常普遍,但其安全性以及对我国结核诊治带来的影响不容忽视,新型抗菌药物的上市将为临床提供更多选择。
笔者获悉,Lefamulin 注射和口服制剂已于 19 年 8 月 19 日获 FDA 批准,用于治疗成人社区获得性细菌性肺炎。上海仑胜医药科技有限公司拥有 Lefamulin(SNV001)大中华地区的开发和营销权利,并已获得国家药品监督管理局批准的临床研究批件,在中国大陆地区开展桥接试验,预计将于 2019 年第四季度开始招募患者。
作者:王业明 首都医科大学呼吸病学系 中日友好医院呼吸与危重症医学科
本网站转载须联系版权方授权



