 文献来自:Chung JH, Walker CM, Hobbs S. Imaging Features of Systemic Sclerosis-Associated Interstitial Lung Disease. J Vis Exp . 2020 Jun 16;(160).doi: 10.3791/60300.
文献来自:Chung JH, Walker CM, Hobbs S. Imaging Features of Systemic Sclerosis-Associated Interstitial Lung Disease. J Vis Exp . 2020 Jun 16;(160).doi: 10.3791/60300. 文献来自:Chung JH, Walker CM, Hobbs S. Imaging Features of Systemic Sclerosis-Associated Interstitial Lung Disease. J Vis Exp . 2020 Jun 16;(160).doi: 10.3791/60300.
文献来自:Chung JH, Walker CM, Hobbs S. Imaging Features of Systemic Sclerosis-Associated Interstitial Lung Disease. J Vis Exp . 2020 Jun 16;(160).doi: 10.3791/60300.马志明编译
摘 要
引 言
方 法
典型结果
诊断
HRCT上SSc-ILD的主要特征通常包括非特异性间质性肺炎 (NSIP),伴有外周磨玻璃影(GGO)和广泛的牵拉性支气管扩张 (图1和图2)。GGO病因广泛,往往呈非特异性[40-42]。好发于中心部位或呈外周分布伴胸膜下不受累提示NSIP (图3)。
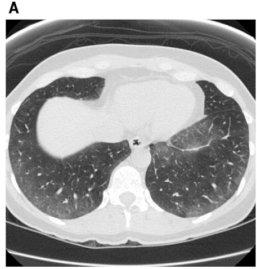
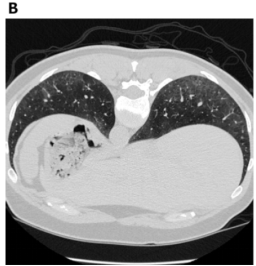
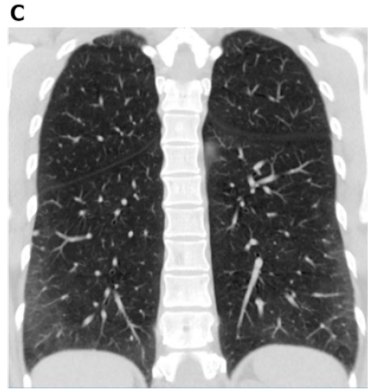
图1: 系统性硬化症伴细胞型NSIP型。轴位 (A) 、俯卧位 (B) 和冠状位 (C) HRCT图像均显示广泛的外周和基底段为主的GGO,提示为NSIP的典型表现。缺乏牵拉性支气管扩张则提示细胞型NSIP型。
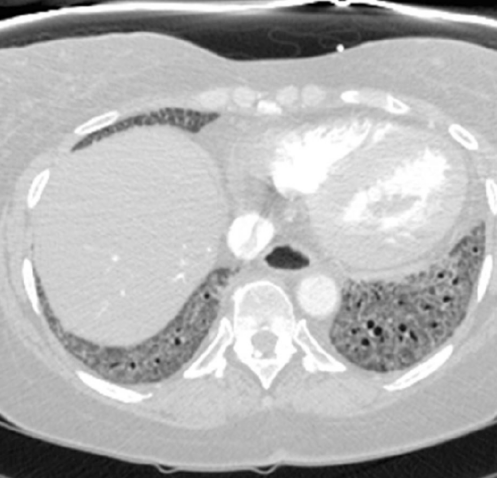
图2: 系统性硬化症伴纤维化的非特异性间质性肺炎类型。轴位位CT图像显示广泛的、以基底段占优势的GGO伴牵拉性支气管扩张。值得注意的是,食管明显扩张,此为典型的硬皮病
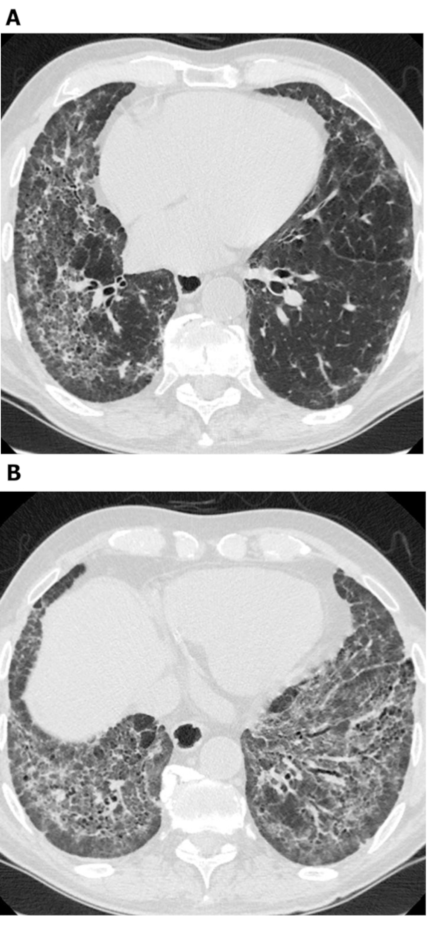
图3: 系统性硬化症伴纤维化NSIP型。轴轴状位CT图像 (A和B) 显示广泛的GGO、网状影、结构扭曲和牵拉性支气管扩张。值得注意的是,胸膜下不受累区较明显,此为典型的NSIP,可见于约50% 的病例。
HRCT影像中的ILD典型表现包括网状影伴结构扭曲导致牵拉性支气管扩张/细支气管扩张 (符合NSIP的纤维化形式)。牵拉性支气管扩张和牵拉性细支气管扩张往往是SSc-ILD的主要特征 (图4)[43]。其他发现可能包括蜂窝征 (图5; 更常见于局限性SSc) 、小叶间隔增厚和小叶内线以及微结节[40,44]。蜂窝征是指具有典型的直径较一致 (3-10mm) 且边界清楚的厚壁聚集性囊性气腔[31]。蜂窝征和牵拉性支气管扩张是HRCT常见的UIP主要特征。尽管这种类型最常与特发性肺纤维化 (IPF) 有关,但有时可在SSc-ILD10患者中见到呈进展性表型的典型纤维化ILD[10]。最近,在结缔组织病相关的ILD (包括SSc-ILD) 患者HRCT上表现为UIP类型中发现了一些征象,但在IPF患者中没有被发现。在头尾切面上存在直边征 (例如肺纤维化与肺基底部的分割线呈税利边界,冠状位上显示未沿肺外周边缘呈实质性延伸),蜂窝征占优势 (或密集) (肺纤维化部分> 70%)。前上叶征 (例如上叶前段的纤维化集聚,上叶其他部分相对减少,并伴随下叶受累) [45]。直边征也与NSIP病理有关[46],这是SSc-ILD10的主要CT表现[10]。
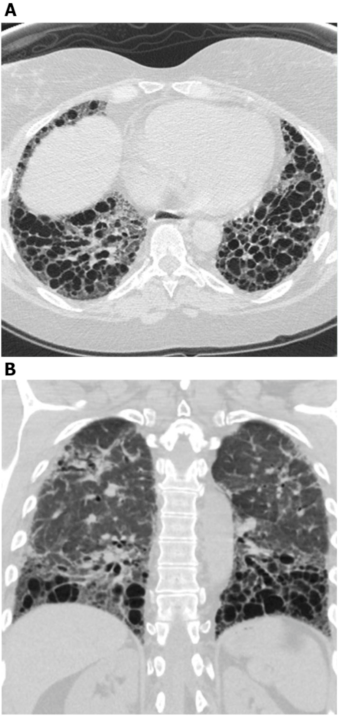
图4. 系统性硬化症伴大量牵拉性支气管扩张。轴状位 (A) 和冠状位 (B) HRCT图像显示广泛的中、下肺野占优势的牵拉性支气管扩张。虽然这可能被误认为蜂窝征,但囊性区域相互连接,且近胸膜下肺区域不受累,此为典型的支气管扩张。
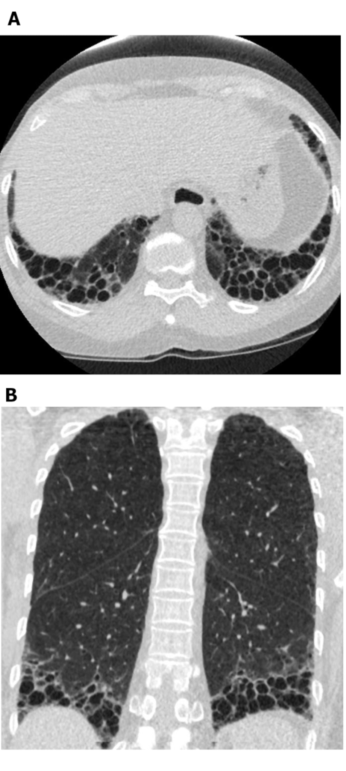
图5: 系统性硬化症伴纤维化的UIP型。轴状位 (A) 和冠状位 (B) CT图像显示外周和基底段占优势的蜂窝征和牵拉性支气管扩张与典型的肺纤维化UIP型一致。注意食管扩张 (归因于硬皮病) 和 “密集” 的蜂窝征 (提示ILD与结缔组织病相关,而不是与特发性肺纤维化相关)。
充气食管扩张常见于 SSc患者 (图6)[47-49]和SSc- ILD患者[47-48]。食管扩张可能不再有助于区分SSc- ILD和IPF,尽管没有公认的年龄上限,但食管扩张可能更难以说明 65岁以上的患者,因为其食管动力障碍的发病率增加。淋巴结肿大 (通常为是反应性),其中淋巴结短轴超过10mm,也常见于患者 SSc-ILD[47,50]。肺动脉直径大于邻近升主动脉提示共存肺动脉高压 (图6),即使在没有纤维化的患者中也是如此[51-53]。实变区提示合并感染、误吸、机化性肺炎、出血或恶性肿瘤。必须监测SSc-ILD患者中的结节影,因为肺癌的风险增加[7]; SSc-ILD患者最常见的原发癌为腺癌[7,54]。
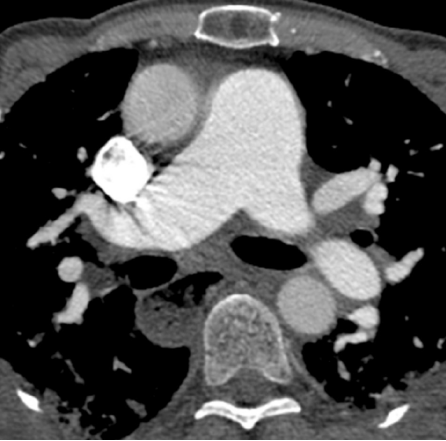
图6: 系统性硬化症伴肺动脉高压和食管扩张。对比增强胸部CT显示肺动脉干明显扩张,其测量值大于邻近升主动脉,提示潜在的肺动脉高压。食管明显扩张,可归因于硬皮病。
SSc-ILD与IPF有许多临床、机制和病理上的相似之处[15,55]。然而,一些影像学特征能够区分这两类ILDs[15,45]。在SSc-ILD中,与IPF相比,GGO比例更大,纤维化的程度更低。在SSc-UIP病例中,70% 以上的纤维化肺组织可观察到蜂窝状结构,即密集旺盛的蜂窝征[56-57]。此外,四角征 (也称为前上叶征) 在SSc-ILD中比在IPF中更为常见; 这是一种炎症和/或局部或不呈比例的纤维化模式,累及双侧上叶前段外侧和下叶后上方[58]。
胸片最初可发现ILD,但不能为可靠的诊断提供足够的对比分辨率。在SSc-ILD患者的胸片中,最常见的表现为基底部为主的网状影[59]。进一步的特征可能见到支气管扩张,肺容积减少和蜂窝状影。与HRCT一样,充气食管扩张可能有助于支持SSc-ILD的诊断[47]。
预 后
一些不同的影像学表现显示与SSc-ILD的预后相关。据报道,HRCT显示病变范围至少20% 的患者死亡风险较高 (病变范围高于或低于20% 阈值的患者中,10年生存率分别为43% 和67%)[60]。同样,HRCT的高纤维化评分 (依据于网状影和蜂窝状影的范围) 与死亡率升高相关[61]。食管直径增大与ILD严重程度增加和DLCO降低有关[48]。肺密度和肺动脉直径可能用于预测肺动脉高压的风险[62]。计算机化的定量CT参数也可用于确定患者肺功能下降或死亡的风险。一项研究表明,来自于HRCT量化的ILD范围可以用来预测12个月后FVC的下降率[63]。在另一项研究中,定量胸部CT参数提供了与临床预测模型相一致的死亡风险结果[64]。尽管这些结果具有明显的潜力,但基于影像的生物标志物目前最好在人群水平上考虑,因为其在个体患者中的临床应用尚未确定。
治疗反应
环磷酰胺和麦考酚酸酯可使SSc-ILD患者轻度获益。在具有里程碑意义的肺硬皮病研究I中,与安慰剂相比,环磷酰胺治疗可延缓纤维化进展[65]。最近,与环磷酰胺比较,肺硬皮病研究II报道了麦考酚酸酯与环磷酰胺66相似的疗效和改善的耐受性[66]。基于阳性的SENSCIS®试验结果[67],尼达尼布成为美国FDA批准的第一种能减缓SSc-ILD患者肺功能下降速度的治疗药物。然而,SSc-ILD患者仍需要改进治疗方案。目前正在研究的治疗方法包括单克隆抗体 (例如利妥昔单抗,阿比珠单抗),抗纤维化药物 (例如吡非尼酮),直接凝血酶抑制剂达比加群,蛋白酶体抑制剂硼替佐米,造血干细胞移植[19,68]。
HRCT系列扫描显示
SSc-ILD患者的疾病进展
在不同时间点进行的HRCT评估可用于研究疾病进展。图7显示了1例SSc-ILD患者间隔10年拍摄的两组轴位和冠状位胸部HRCT图像。胸部HRCT的初始轴位和冠状位图像 (图7A和B) 显示基底部占优势的GGO和网状影伴轻度牵拉性支气管扩张和胸膜下不受累区,与SSc患者的NSIP一致。后一组10年后拍摄的轴位和冠状位胸部CT图像 (图7C和D),显示肺基底部网状影和牵拉性支气管扩张增加,GGO减少 (图7C和D),与肺纤维化轻度进展相一致。连续的HRCT扫描也可用于监测治疗反应[69,70,71]; 这在硬皮病肺研究II中得到证实,其中基于HRCT扫描的计算机辅助诊断评分用于比较环磷酰胺和霉酚酸酯对SSc-ILD69患者的疗效。
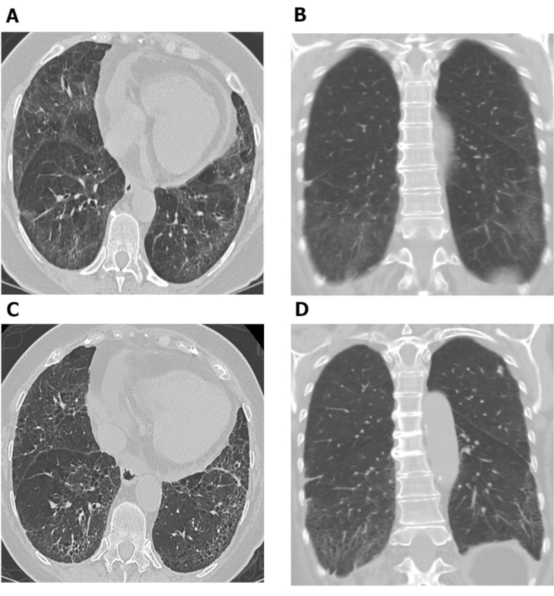
图7: 连续胸部HRCT图像显示SSc-ILD患者的肺纤维化进展。轴状位 (A) 和冠状位 (B) 胸部HRCT图像显示基底段占优势的GGO和网状影,伴轻度牵拉性支气管扩张和胸膜下不受累区,与SSc患者的NSIP型相一致。10年后,轴状位 (C) 和冠状位 (D) 胸部HRCT图像上观察到肺基底段网状影和牵拉性支气管扩张增加,GGO减少,与肺纤维化轻度进展相一致。
讨 论
虽然HRCT是目前诊断和评估SSc-ILD的确定性影像方法,但存在电离辐射,价格相对昂贵。虽然不能像HRCT那样有助于鉴别诊断,但也可以改为胸片,正常的胸片不能排除ILD的可能性。也许胸片最好使用在HRCT扫描之间以监测疾病的进展,并在症状急性加重的情况下排除并发症,如感染性肺炎。
HRCT的一个缺点是辐射暴露。如前所述,CT扫描的新方法可以减少辐射暴露[31]。目前的CT扫描机提供了一系列先进技术,为将来辐射暴露降低到接近胸片水平提供了可能性。另一种成像方法,如MRI或肺超声可以潜在地用于将来避免患者辐射暴露[32,72-74]。我们相信,虽然存在与影像学应用相关的风险效益考虑,但CT在诊断和患者管理方面的优势远远超过了潜在的风险。
影像资料,尤其是HRCT,为SSc-ILD的诊断提供了最重要的信息。详细考虑HRCT扫描的模式和特征通常足以区分SSc-ILD和其他肺部疾病,从而避免需要有创性性活检。
HRCT扫描的视觉评估引入了一定程度的主观性和观察者之间差异的可能性。基于计算机的HRCT扫描解释方法已被研究为提高精准性的一种可能性方法[63,75]。例如,评估肺纤维化或疾病范围的定量方法可用于评估治疗反应[69,71,76]。然而,这些方法目前尚未广泛应用于日常临床实践。
利益冲突披露
声明本文所描述的研究、作者和/或文献发表没有潜在的利益冲突; Christopher Walker声明收到阿米尔西斯 (Elsevier) 的特许权使用费; Stephen Hobbs声明收到Elsevier和Wolters Kluwer健康公司的特许权使用费。这篇文章的公开发表是由勃林格殷格翰制药公司赞助的。
参考文献:略
图文编辑:刘宏宇




